Escinco de bandas
Scincopus fasciatus (Peters, 1864)
Por Pablo García-Antón, Alberto Sánchez-Vialas, Javier Lobón-Rovira, Fernando Iglesias &Teodoro Abbad
Actualizado: 09/02/2023
Taxonomía: Scincoidea | Scincidae | Scincopus | Scincopus fasciatus

 Scincopus fasciatus
Scincopus fasciatus
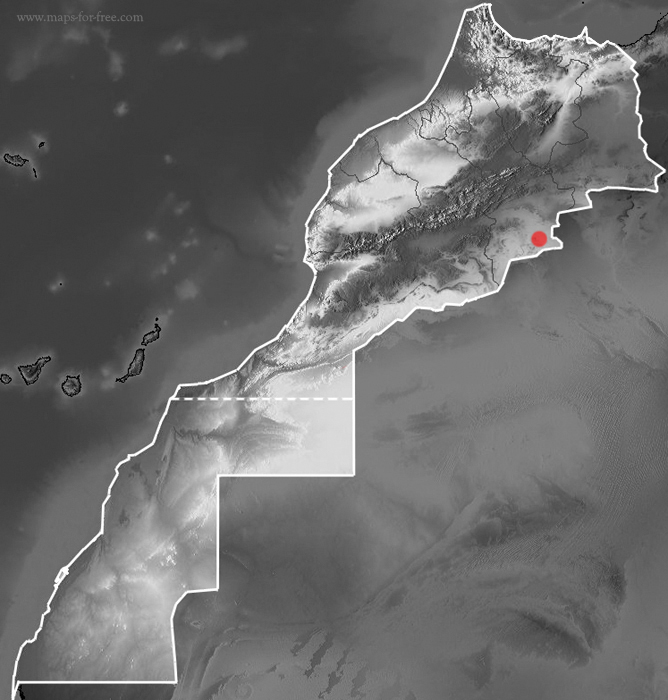
Mapa de distribución conocida de Scincopus fasciatus en Marruecos.
1) Encuadre filogenético
Scincopus Peters, 1864 es un género monoespecífico de escíncidos (familia Scincidae Oppel, 1811) representado por la especie Scincopus fasciatus (Peters, 1864), que a su vez comprende dos subespecies tradicionalmente reconocidas: S. f. fasciatus, distribuida en la mayor parte del rango geográfico que ocupa la especie y S. f. melanocephalus Lanza & Corsi, 1981, conocida exclusivamente del lado Este del río Nilo en Suakin, noreste de Sudán, y cuyo estatus taxonómico es incierto.
Las relaciones filogenéticas basadas en datos moleculares sugieren una estrecha relación entre S. fasciatus y E. algeriensis, poniendo de manifiesto que el género Eumeces es paráfilético (E.algeriensis se encuentra más emparentado con Scincopus que con la otras especies de Eumeces), evidenciando la necesidad de una revisión taxonómica de este grupo (Carranza et al., 2008; Perea et al., 2012; Zheng & Wiens, 2016).

2) Descripción
Scincopus fasciatus destaca entre el resto de especies de eslizones marroquíes por reunir una serie de características morfológicas únicas, descritas a continuación.
De complexión general robusta y cilíndrica, su longitud hocico-cloaca (SVL) oscila alrededor de los 15 cm, aunque llega a alcanzar los 24 cm de longitud total (Martínez del Mármol et al., 2019). Los juveniles recién nacidos miden en torno a 6 cm (de longitud total) y 3,5/ 4 cm de (SVL) (Sánchez-Vialas et al., 2022).
Cabeza con forma ovalada y ligeramente distinta del cuello, presenta grandes ojos negros, ribeteados en su contorno con ciertas tonalidades negras y sin pupila discernible. La folidosis de la cabeza se caracteriza principalmente por la siguiente combinación de escamas: escama rostral moderadamente grande (característico de reptiles con hábitos hipogeos) en contacto con las nasales, 6 supraoculares; parietales del mismo tamaño que las interparietales, cuatro pares de escamas nucales, región loreal con una escamado redondeado; 9 supralabiales, sobresalientes hacia afuera en su parte inferior donde la quinta y la sexta se encuentran debajo del ojo; 7 Infralabiales; un gran disco palpebral translúcido compuesto por un escamamado poligonal. Cavidad timpánica enmascarada con 2 grandes escamas sobresalientes (Schleich et al., 1996). Ojo parietal claramente definido (observación personal de los autores).


Tronco cilíndrico, robusto y relativamente alargado, recubierto de un escamado liso y brillante. No existe apenas diferencias entre ambas subespecies en cuanto a número de escamas alrededor del cuerpo, presentando entre 23-26 hileras longitudinales alrededor del cuerpo en su parte central (Martínez del Mármol et al., 2019). El escamado dorsal se encuentra estriado longitudinalmente con 2 o 3 surcos que atraviesan las escamas en todo su largo, las dorsales el doble del tamaño de las ventrales (Schleich et al., 1996). Región anterior de los costados con sinuantes hendiduras donde se sitúan las extremidades anteriores durante sus desplazamientos bajo el sustrato. Extremidades cortas, robustas y pentadáctilas con dígitos apenas agrandados.
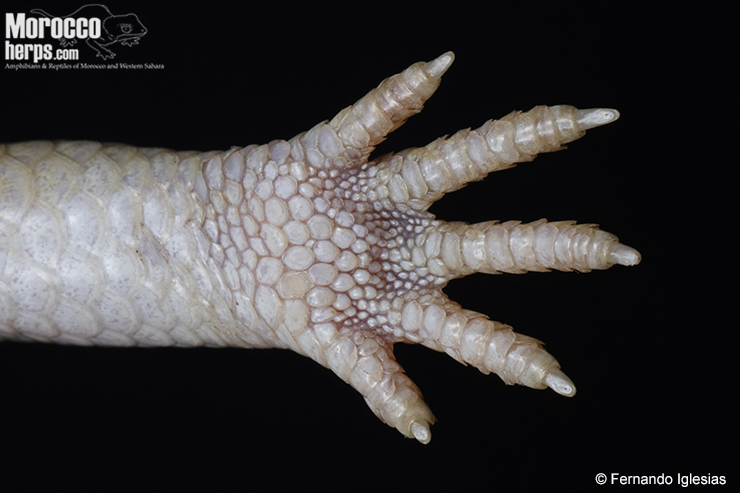
Cola robusta corta y cónica, de sección relativamente circular y dos veces más corta que el cuerpo (Martínez del Mármol et al., 2019). En la región cloacal existen dos grandes placas anales (Trape et al., 2012). Esta especie presenta autotomía caudal (Schleich et al., 1996).
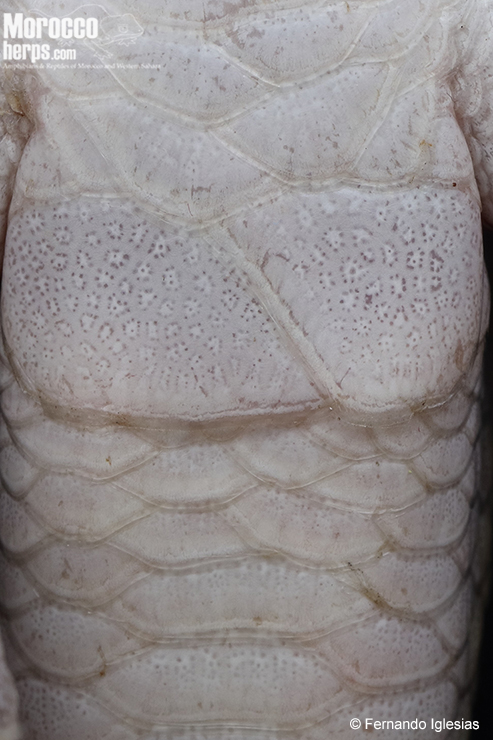
Poros preanales ausentes en ambos sexos. Dimorfismo sexual poco marcado: machos con tallas más grandes y cabezas más robustas (Schleich et al., 1996). Las hembras por regla general presentan las placas anales fusionadas, conformando una gran placa cubriendo la sutura cloacal (observación personal de los autores). Los machos presentan hemipenes bilobulados en sus extremos (observación personal de los autores).
La coloración dorsal de fondo es generalmente amarillenta–anaranjada, sobre este plano dorsal destacan con mayor o menor intensidad una serie de franjas transversales negras entre 5-8 que pueden ser más pequeñas que los espacios intermedios o de aproximadamente el mismo ancho (Schleich et al., 1996). La punta de la cola es negra total o ribeteada de negro a través de su contorno en función del individuo. La parte ventral es de tonos blanquecinos (Schleich et al., 1996).
Existen dos fenotipos en S. fasciatus que han sido tratados como rasgos diagnósticos de las subespecies descritas. Lanza y Corsi (1981) observan diferencias significativas entre ambas subespecies en base a su patrón de coloración. La forma nominal Scincopus f. fasciatus, presenta la parte superior de la cabeza ausente de coloración negruzca o con escasas marcas oscuras dispersas, los lóbulos laterales de la cabeza sin manchas o con tenues marcas de color negruzco. El bandeado transversal del plano dorsal siempre bien desarrollado. La forma S. f. melanocephalus presenta tanto la parte superior como la lateral de la cabeza completamente negra, la región gular con algunas manchas oscuras o un moteado difuso oscurecido, bandas transversales oscuras a veces ausentes y generalmente menos desarrolladas.

Los juveniles presentan un patrón de coloración dorsal similar a los adultos pero con tonos más apagados o pálidos, sobre el que destacan las franjas negras mucho más contrastadas, conformando el característico diseño de los adultos.

Osteología
El cráneo no difiere del patrón general de los escíncidos. Se encuentra ligeramente aplanado dorsoventralmente, y altamente reforzado, debido a un alto grado de solapamiento entre sus estructuras óseas. Presenta 24 dientes pleurondontos-isondotos en la maxila y 6 en la premaxila. Cavidad ocular bien delimitada anteriormente por los huesos frontales, prefrontales y maxilares, y posteriormente por los huesos jugales, frontales y postfrontales. Cabe destacar 5 o 6 perforaciones simétricas en la región medial del hueso pterigoideo. Presenta una fontanela supratemporal ancha. Hueso cuadrado bien desarrollado, marcadamente curvado antero-dorsalmente. Palatino estrecho, ensanchándose anteriormente donde contacta ampliamente con la maxila. Huesos de la cavidad cerebral fusionados, típico de escíncidos. El espécimen aquí descrito presenta 26 vertebras presacras, las dos primeras carentes de costillas desarrolladas (cervicales), lo que es acorde a los resultados encontrados por Griffith et al. (2000). Sugerimos la necesidad de este tipo de estudios osteológicos en individuos de temprana edad para ver si existen diferencias directas en la forma de los elementos osteológicos craneales y la edad como ocurre en Eumeces schneideri (Yildirm et al., 2015).
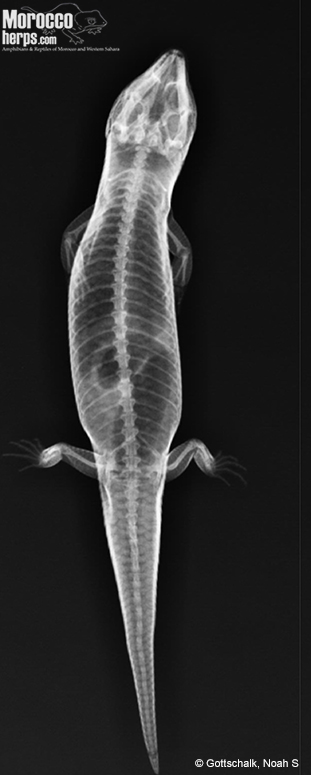
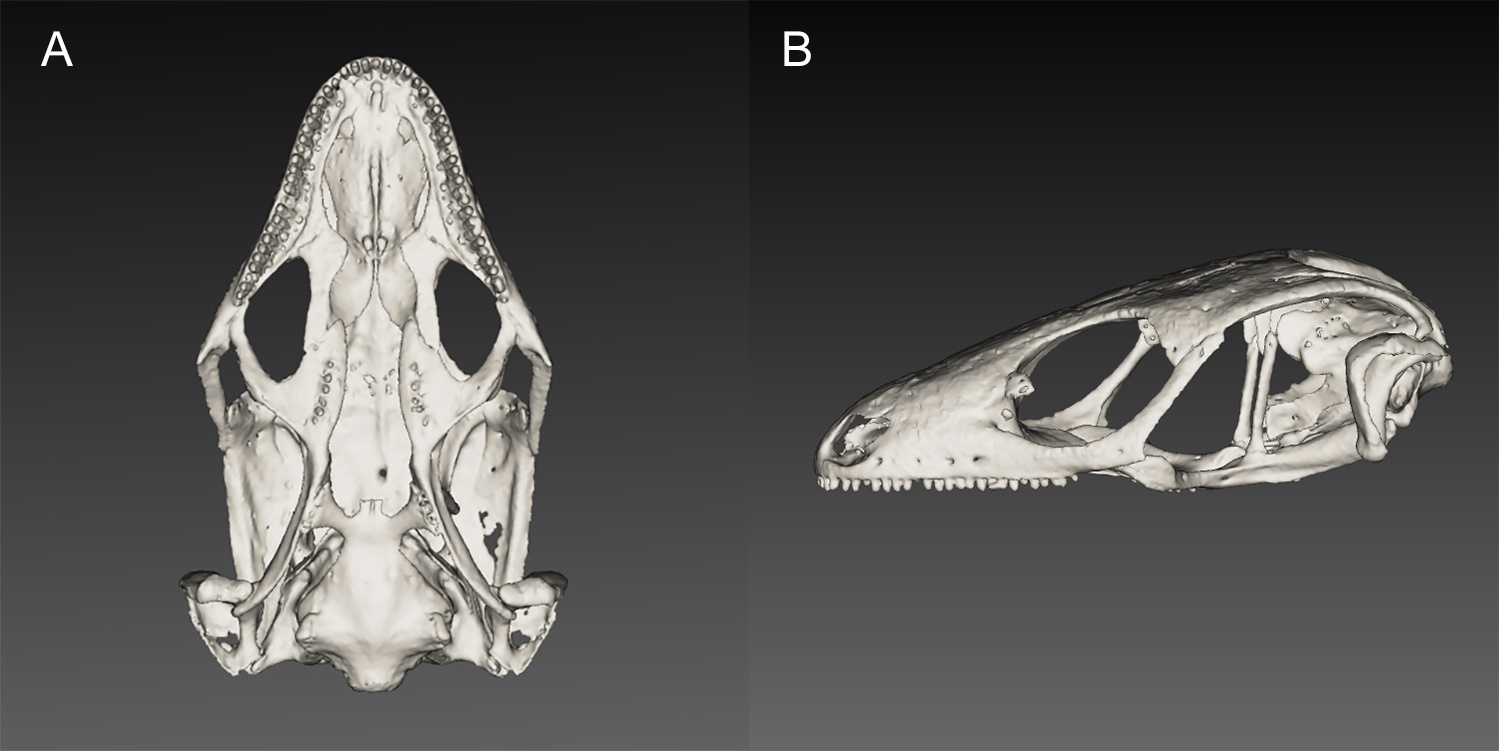
El escamado del género Scincopus, al igual que en otros representantes de hábitos hipogeos, presentan altos contenidos en β-queratina. Esta mayor densidad del componente mencionado en las escamas puede protegerlo de la abrasión por la fricción de la arena mientras se desplaza (Staudt et al., 2012)
3) Ecología y hábitos
Scincopus fasciatus es una especie estrictamente nocturna, de hábitos crípticos, veloz, ágil, y eminentemente fosorial que pasa la mayor parte del tiempo bajo el sustrato arenoso. Se desplaza a gran velocidad por los hábitats que ocupa. Se puede encontrar al cobijo de formaciones rocosas y en general cerca de plantas con porte bajo, en ocasiones con pinchos que le dan mayor seguridad a sus refugios. Es capacez de recorrer largas distancias (más de 200 m), para luego regresar a su mismo refugio de partida (Kalboussi et al., 2021).
En cuanto a su biología reproductiva, se trata de una especie ovípara (Sánchez-Vialas et al., 2022). Los datos conocidos del período de ovoposición en el género Scincopus proceden de observaciones realizadas en cautividad. Los apareamientos tienen lugar en el mes de febrero (Sánchez-Vialas et al., 2022). La puesta de huevos tiene lugar entre los meses de marzo y abril.
Se ha reportado un total de 5 huevos de 2.5 x 1.3 cm que eclosionaron tras un periodo de incubación de entre 40-45 días a 32ºC y 80% de humedad (Sánchez-Vialas et al., 2022). La primera muda se realiza a los 8 días del nacimiento y se desarrollan lentamente hasta alcanzar el estado adulto, tardando aproximadamente cuatro años (Sánchez-Vialas et al., 2022). En Túnez se encuentran juveniles durante junio-julio (Kalboussi et al., 2021).
Especie probablemente territorial durante el período de apareamiento, época en que los machos desarrollan una marcada actividad nupcial (Kalboussi et al., 2020).

Scincopus fasciatus es principalmente un merodeador activo, capaz de captar las vibraciones de las presas en el terreno y detectar insectos a una distancia de 15 cm en la oscuridad (Scheich et al., 1996).
Se alimenta principalmente de invertebrados, no obstante, en ciertas ocasiones puede llegar a alimentarse de vertebrados como escíncidos del género Scincus (Martínez del Mármol et al., 2019). El alimento vegetal podría formar una parte importante de su dieta, consistiendo en vainas jóvenes de especies como Retama raetam Webb & Berthel (observación personal de los autores).
No se conocen depredadores, aunque es posible que algunas de las especies de mamíferos con las que comparte hábitat, como la zorrilla norteafricana (Ictonyx libyca) o el erizo del desierto (Paraechinus aethiopicus)(F. Iglesias, obs. pers.), puedan alimentarse de ellos. En el sur de Mauritania comparte hábitat también y posiblemente refugio con la gariba (Echis leucogaster)(A. Izagirre, S. Frahm, M. Sassoe & G. Martínez del Mármol, datos inéditos) por lo que, tratándose de un ofidio con un amplio abanico de presas, es probable que se alimente de los juveniles de Scincopus fasciatus.


4) Distribución, hábitat y abundancia
Scincopus fasciatus presenta una fragmentada distribución entre la Zona de Transición Regional Submediterránea y la Zona de Transición Regional del Sahel (Wickens et al., 1984) extendiéndose a través de Mauritania, Mali, Níger, Norte de Nigeria, Chad hasta Sudán (Martínez del Mármol et al., 2019). Su posible presencia al norte de Senegal es señalada (Vicent-Castelló et al., 2018).
Con respecto a su distribución magrebí, presenta poblaciones en Marruecos, Algeria, Túnez y Libia, estando totalmente ausente en Egipto (S. Baha El Din, com. pers) (ver Tabla debajo).
| Country | Locality | Latitude | Longitude | Reference |
| Algeria | Ayata Lake | 33.488056° | 5.986111° | Chenchouni et al. (2012) |
| Algeria | El Bayadh | 33.685390° | 1.030340° | Lanza & Corsi, 1981 |
| Algeria | Oued souf | 33.685355° | 1.030317° | Abdelhadi et al. (2018) |
| Algeria | Touggourt | 33.104928° | 6.066273° | Lanza & Corsi, 1981 |
| Algeria | Taibet | 33.082745° | 6.398630° | Lanza & Corsi, 1981 |
| Algeria | Tindouf | 27.687512° | -8.117491° | Geniez et al. (2004) |
| Algeria | Mountains of Eglabs | 26.416111° | -5.225555° | Geniez et al. (2004) |
| Chad | Abeche | 13.835912° | 20.843370° | Lanza & Corsi, 1981 |
| Libia | Badr: Al-Bedair | 32.04083° | 11.54389° | Ineich et al. (2005) |
| Libia | Bishr | 30.35700° | 19.19400° | Bauer et al. (2017) |
| Libia | Badr ( Al-Bedair) | 32.043022° | 11.536172° | Ibrahim et al. (2005) |
| Libia | Tripoli | 32.78455° | 13.21437° | Sindaco et al. (1995) |
| Mali | Goundam | 16.417560° | -3.664866° | Lanza & Corsi, 1981 |
| Mali | Timbuktu | 16.766547° | -3.002576° | Lanza & Corsi, 1981 |
| Mauritania | 15 km N Nouakchott Airport | 18.231483° | -15.946002° | GBIF |
| Mauritania | El Haédi | 16.606504° | -15.897594° | Vicent-Castelló et al .(2018) |
| Mauritania | Lahouvich | 16.633233° | -15.983350° | Trape et al. (2012) |
| Mauritania | Nterguent | 28.017309° | -0.264305° | Geniez et al. (2004) |
| Mauritania | Trarza : La’ Bâra | 18.758496° | -15.266712° | Le Berre et al. (1989) |
| Mauritania | Trarza: near Tiguent | 17.244110° | -15.991393° | Böhme et al. (2001) |
| Mauritania | Nuakchot | 18.073529° | -15.958237° | Böhme et al. (2001) |
| Mauritania | Boutilimit | 17.866022° | -14.659588° | Lanza & Corsi, 1981 |
| Marreucos | Taouz | 30.906754° | -3.996144° | Bons & Geniez, 1996 |
| Niger | Guesselbodi: 30 km SE Niamey | 13.413166° | 2.353500° | GBIF |
| Niger | Tillabéry: Ouallam | 14.516667° | 1.933333° | GBIF |
| Niger | 50 km E of In Gall | 16.786713° | 6.934322° | Lanza & Corsi,1981 |
| Niger | Agadez | 16.974126° | 7.986515° | Angel & Lathe (1938) |
| Niger | Arlit | 18.693494° | 10.982057° | GBIF |
| Niger | Bilma | 18.692960° | 12.917650° | Angel & Lathe (1938) |
| Niger | Danga Village | 14.493840° | 1.903241° | Lanza & Corsi, 1981 |
| Niger | Kaouar | 19.082884° | 12.866569° | Angel & Lathe (1938) |
| Niger | Kélakam: 10km W of Diffa | 13.562232° | 11.661053° | Gonçalves et al. (2013) |
| Niger | Niamey | 13.511500° | 2.125343° | Lanza & Corsi, 1981 |
| Niger | Tahoua | 14.890385° | 5.257965° | Trape et al. (2012) |
| Niger | Tasker: 8km S of Zinder | 15.081673° | 10.632372° | Gonçalves et al. (2013) |
| Niger | Termit: Louli Agadem Nga | 16.181.423° | 11.319161° | Gonçalves et al. ( 2013) |
| Niger | Termit: Madaranga | 15.872192° | 11.446412° | Gonçalves et al. (2013) |
| Niger | Aïr Massif | 18.280000° | 8.000000° | Ineich et al. (2014) |
| Niger | Gaon,ear In Tezentes | 17.432130° | 6.638349° | Angel & Lathe (1938) |
| Niger | Boboye | 12.433863° | 2.890236° | GBIF |
| Niger | Kouré | 13.325358° | 2.591644° | Chirio et al. (2009) |
| Niger | Diffa | 13.5622º | 11.6611º | Velo-Anton et al. (2022) |
| Niger | Zinder | 15.0817º | 10.6324º | Velo-Anton et al. (2022) |
| Niger | Tessaoua | 13.755716° | 7.986473° | Lanza & Corsi, 1981 |
| Nigeria | Zamfara Valley | 11.494093° | 4.233313° | Lanza & Corsi, 1981 |
| Nigeria | Sokoto & Kware | 13.005594° | 5.247469° | Lanza & Corsi, 1981 |
| Sudan | Barah | 13.698504° | 30.372324° | Werner et al. (1919) |
| Sudan | Kharthoum | 15.500597° | 32.559869° | Boulenger et al. (1887) |
| Sudan | Suakin | 19.103974° | 37.329254° | Anderson et al. (1896) |
| Sudan | Wad Banda | 13.089911° | 27.942457° | Lanza & Corsi, 1981 |
| Tunez | 40 km NW Sfax | 34.739553° | 10.759983° | Schleich et al. (1996) |
| Tunez | Hazua Oasis :35 km west of Nefta | 33.876086° | 7.880325° | Lanza & Corsi, 1981 |
| Tunez | Metlaoui : 42 km WSW of Gafsa | 34.319300° | 8.407417° | Sindaco et al. (1995) |
| Tunez | Sidi-Guenao: S of Gabes | 33.887875° | 10.097398° | Lanza & Corsi, 1981 |
| Tunez | South of Chott el Djerid | 33.778072° | 8.396453° | Sindaco et al. (1995) |
| Tunez | Tozeur: plain of Arad S Gabes | 33.918480° | 8.122923° | Schleich et al. (1996) |
| Tunez | Arad Plain : S of Gabes | 33.888077° | 10.097522° | Kalboussi et al. (2020) |
| Tunez | Souk Djedid | 34.941948° | 9.561784° | Nouira et al. (1999) |
| Tunez | chott el Djerid | 33.778216° | 8.396493° | Blanc C.P. & Shane M.H. (1981) |
| Tunez | BouHedma National Park | 34.471935° | 9.478381° | Kalboussi et al. (2020) |
| Tunez | Douz | 33.461435° | 9.029470° | Kalboussi et al. (2021) |
| Tunez | Jemna | 33.573344° | 9.018418° | Kalboussi et al. (2021) |
| Tunez | Bchelli | 33.616937° | 8.916353° | Kalboussi et al. (2021) |
| Tunez | Regim Maatoug | 33.325387° | 8.013794° | Kalboussi et al. (2021) |
| Tunez | Regueb | 34.858560° | 9.784600° | Kalboussi et al. (2021) |
| Tunez | Mezzouna | 34.577385° | 9.843186° | Kalboussi et al. (2021) |
| Tunez | Sidi Bouzid | 35.035438° | 9.483939° | Kalboussi et al. (2021) |
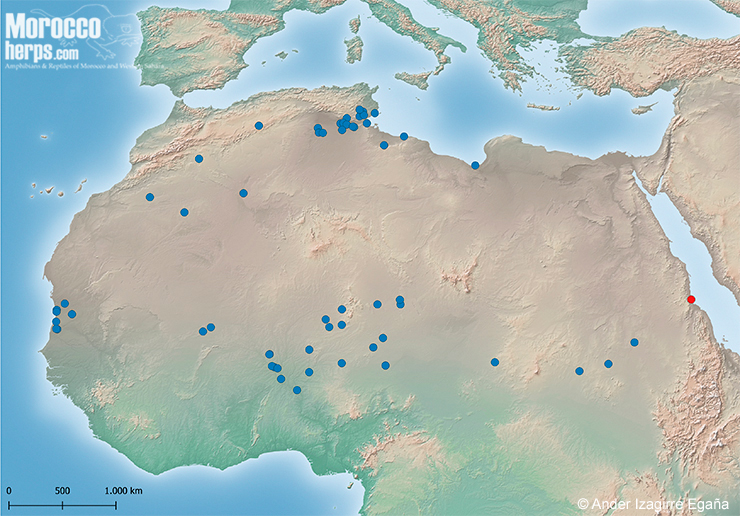
Por cuestiones biogeográficas su presencia en Marruecos se considera altamente probable. En el país de estudio ha sido reportada por un solo espécimen en la región de Draa-Tafilalet en la localidad de Taouz detectado por Yves Vial en 1970 (Martínez del Mármol et al., 2019), donde no se ha localizado desde entonces. Debido a su naturaleza críptica y elusiva, sus avistamientos son poco frecuentes y dispersos por lo que la programación de muestreos más exhaustivos en diferentes periodos estacionales serían necesarios para confirmar su presencia en Marruecos y mejorar el conocimiento corológico de la especie en cuestión.
Con respecto a las dos subespecies designadas para Scincopus fasciatus, se observa una clara distribución alopátrica. En Marruecos (Taouz) y noreste de África (Algeria, Túnez, Libia) subyace la subespecie nominal, S. f. fasciatus (Peters, 1864), además de abarcar ampliamente la región sur del Sáhara a lo largo de las ecorregiones del Sahel. Por otro lado S. f. melanocephalus (Lanza & Corsi, 1981) se conoce de una sola población asentada al este del río Nilo en Suakin, al noreste de Sudán.
Scincopus fasciatus ha sido reportado en varios tipos de hábitats desde regiones arenosas caracterizadas por condiciones climáticas áridas y fuertemente estacionales hasta áreas de sabana en la zona ecoclimática saheliana-sudanesa (Trape et al., 2012; Martínez del Mármol et al., 2019).
En la región de Taouz (Marruecos) esta enigmática especie podría habitar los suelos arenosos cubiertos con vegetación arbustiva dispersa, cordones dunares y amplias planicies con Ergs aislados. En las localidades tunecinas esta especie se encuentrada asociada a especies vegetales tales como Retama raetam, Ziziphus loto, Rhanterium suaveolens, Haloxylon schmittianum y Haloxylon scoparium (Kalboussi et al., 2020).
Las localidades del norte del Sáhara donde habita esta especie se encuentran en áreas donde la precipitación media anual oscila entre 50 y 150 mm, mientras que en las localidades del Sahel, la especie vive en zonas donde la precipitación media anual oscila entre 20 y 500 mm (Sindaco et al., 1995).
Con respecto al rango altitudinal que ocupa, se encuentra a 750 m, atendiendo al único reporte existente en Marruecos (Martínez del Mármol et al., 2019).


Conservación
Entre los factores de amenaza que conciernen a esta especie, destaca la captura directa para el tráfico de especies promovido por el mercado que genera la terrariofilia (observación personal de los autores), como ocurre con otras poblaciones silvestres de múltiples especies extirpadas de su hábitat (observación personal de los autores).
La sobreexplotación insostenible actual y la que se ha venido realizando en los últimos años de las poblaciones silvestres de Scincopus fasciatus para abastecer el mercado de mascotas “animal de compañía” por parte de las granjas o centros en los países exportadores presentes en África puede tratarse como una de las principales causas de su declive poblacional que se enfrenta esta críptica especie (D’Cruze et al., 2020).


Las brechas pronunciadas en la regulación de este comercio no regulado pero legal está suponiendo el colapso de múltiples poblaciones silvestres a nivel mundial acrecentando vertiginosamente la actual crisis de biodiversidad (Faith & Walker et al., 2002).
Uno de los problemas principales estriba en la falta de mecanismos adecuados de control. La estrategia de conservación de la biodiversidad no resulta suficiente por cuanto no establece restricciones con su correspondiente reflejo en las normativas de carácter ejecutor. En la actualidad solo hay una norma que interviene directamente sobre este tipo de comercio. Se trata de la CITES. Esta Convención, en vigor desde el 1 de enero de 1975, regula las transacciones comerciales de importación, exportación y reexportación de especímenes vivos, muertos y sus derivados, de animales y plantas que pueden ver afectada su pervivencia por un comercio no controlado. Cumpliendo, pues, los requisitos de la Convención, que no prohíbe, pero sí regula, la comercialización de animales y plantas sería esperable reducir significativamente la presión sobre la biodiversidad.
Paralelamente a la implementación de la CITES, España ha venido desarrollando una interesante normativa de conservación entre la que cabe destacar además de la Ley 42/2007 el Real Decreto 630/2013, de 2 de agosto, por el que se regula el Catálogo español de especies exóticas invasoras. Sin embargo, la regulación que incorpora no limita ni controla la tenencia de especímenes de especies potencialmente invasoras en España, quedando una puerta abierta a su proliferación para fines particulares, bien de colección, de intercambio o de otro tipo de aprovechamiento.
Ninguno de los textos normativos referidos ha alcanzado el nivel de eficacia presumible para el control de las transacciones de especies exóticas. De hecho, la gran mayoría de éstas no se hallan reguladas en los Apéndices de la CITES. Algunos autores (Auliya et al., 2016) señalan que entre 2004 y 2014 se importaron más de 20 millones de reptiles CITES a los estados miembros de la UE, generando problemas en la sostenibilidad de las poblaciones en su hábitat natural. La perspectiva del comercio de exóticas como mascotas es creciente y significativa. Una estimación basada en datos oficiales asegura que en la UE los hogares en los que habita una mascota alcanzan los 85 millones, lo que da una idea de su envergadura (Toland et al., 2020).
La presencia de animales capturados sin ningún tipo de control sanitario expuestos en diversas ferias tales como Hamm (Alemania), Expoterraria (Madrid y Barcelona), Houten, etc., además de en ciertas instituciones Zoológicas, colecciones privadas, tiendas (observación personal de los autores), suponen un claro detonante para futuras pandemias y eliminación de barreras frente a futuros virus zoonoticos. Siendo por tanto una de las principales vías de enfermedades zoonóticas el actual comercio no regulado pero legal tras lo precedido de la pandemia de COVID-19 (Moorhouse et al., 2021).

La destrucción de su hábitat a través de todo su rango, junto con la recolección por parte de la gente local como atractivo turístico, son otros de los causas de amenaza a los que se enfrenta las poblaciones de esta especie (Geniez et al., 2010). Además, los habitantes de diferentes regiones de Túnez y Níger causan gran número de muertes debido al miedo injustificado de la especie debido a su creencia de posible trasmisión de enfermedades de la piel (Chirio et al., 2009; Kalboussi et al., 2021).

Además, la escasez de datos biológicos debido a su baja probabilidad de detección hace necesario el desarrollo de estudios que permitan ampliar los registros de S. fasciatus tanto a lo largo de las localidades conocidas como en otras áreas donde potencialmente podría encontrarse esta especie y aumentar el conocimiento de su historia natural, tal que permitan plantear estudios para conocer la dinámica poblacional, requerimientos específicos de hábitat y uso de recursos con el objetivo de reevaluar su estado de conservación el cual se encuentra catalogado actualmente por la UICN como “preocupación menor” (Geniez et al., 2010).
Así pues, las cuestiones más relevantes respecto a la tenencia de especies exóticas como animales de compañía radican, en primer lugar, en la situación de partida, es decir en la, muchas veces, escasa información sobre las poblaciones nativas y la potencial afección por la presión comercial, sin que existan en general estudios suficientes sobre su sostenibilidad. Por otra parte, y ya en destino, podemos sintetizar la problemática en la disponibilidad por parte del propietario de gozar de espacio adecuado en función de las necesidades del animal y conocimientos para su mantenimiento, la posible transmisión de zoonosis y epizootias y el problema del escape e instalación de la exótica entre la fauna silvestre autóctona, todo ello sin contar con otros problemas asociados al abandono, como los célebres casos de tortuga de florida o cotorra argentina, entre otros.
En 2020 se creó la Dirección General de Derechos de los Animales con la misión básica de desarrollar una normativa que asegure los derechos, protección y bienestar de los animales que no son, en general objeto de otra regulación. Uno de los elementos que más honda preocupación generaba en el planteamiento del anteproyecto de Ley (en adelante, APL) era la problemática del abandono y escape no controlado de animales de compañía, en las diferentes vertientes de la misma, entre las que se incluían las posibles afecciones a la conservación de la biodiversidad. Por ello, recogiendo los avances y tentativas que se han ido generando en otros foros en los últimos años, se ha habilitado en el APL un capítulo dedicado a la creación y gestión de un Listado Positivo de animales de compañía que permita identificar qué animales se pueden adquirir para su tenencia como animales de compañía, pero con determinadas condiciones.
Previamente a los trabajos para la inclusión del Listado Positivo en el texto del APL ya se había formado una fuerte corriente de opinión liderada en Europa por el “Eurogroup for animals”, plasmada en diversos textos al respecto señalando la importancia y conveniencia de un listado positivo de animales de compañía, y que en España ha tenido impulso y apoyo significativo en la Coalición por el listado positivo.
La lista positiva ofrece como ventajas, no solo su carácter más concreto frente a un listado negativo, sino que además incorpora mayor seguridad jurídica, permite asegurar las condiciones de tenencia mínimas que garanticen la protección de los animales y además posibilita minimizar los efectos negativos sobre la conservación de la biodiversidad.
La garantía de este listado radica en que su desarrollo se efectuará desde un Comité Técnico y Científico que analizará la información disponible de cada especie para la que se solicite su inclusión. Este Comité se desarrollará reglamentariamente, naciendo con espíritu abierto en la composición y esquema genéricos de funcionamiento. En este funcionamiento se establecerán los requisitos de forma y de fondo que debe reunir una especie y el lugar de destino para poder formar parte del Listado Positivo, y que al menos deberán asegurar que:
– Los animales del Listado Positivo deberán ser susceptible de mantenerse adecuadamente en cautividad y los cerramientos o alojamientos donde vivan o estén albergados deberán reunir condiciones apropiadas para que puedan desarrollar sus necesidades fisiológicas, etológicas y ecológicas básicas.
– Deberá existir documentación científica de referencia o información bibliográfica disponible y suficiente sobre el adecuado alojamiento, mantenimiento y cuidado en cautividad del animal en particular. Ello implica conocimiento sobre la especie, su hábitat, sus necesidades básicas y el estado de las poblaciones en origen.
– No se incluirán en el Listado Positivo especies para las que exista certeza de su carácter invasor o que, en caso de escape y ausencia de control, supongan o puedan suponer un riesgo grave para la conservación de la biodiversidad en el ámbito territorial del lugar de tenencia, teniendo en cuenta el principio de precaución.
– No se incluirán en el Listado Positivo animales de especies amenazadas de extinción o vulnerables incluidas en el Catálogo Español de Especies Amenazadas o en los Catálogos regionales de las comunidades autónomas y ciudades de Ceuta y Melilla.
– No se incluirán en el Listado positivo aquellas especies de animales respecto de los cuales existan dudas razonables acerca de la posibilidad de mantenerlas y cuidarlas adecuadamente en cautividad, y no cabrá aplicar medidas de control poblacional con resultado de muerte o aprovechamiento cinegético.
Si bien la confección de este listado, que tiene un carácter dinámico, comporta dificultades para su puesta en marcha se espera que su paulatino asentamiento suponga tanto una mejora en las condiciones de bienestar de los animales, una mejora en el concepto de tenencia responsable y una notable minimización de afecciones significativas en las poblaciones nativas, así como evitar el efecto de las especies exóticas invasoras en la conservación de la biodiversidad autóctona, y supone en todo caso la primera acción normativa directamente encaminada a conseguir los fines citados.
Agradecimientos
A Ander Izagirre Egaña, por el mapa de distribución mundial de la especie.
Bibliografía
- Abdelhadi D, Mhamed S & Louiza A. 2018. Contribution about the environment of El-Bayadh region in the southern-west of Algeria. Advances in Environmental Biology, 12(4): 1-5.
- Anderson J. 1896. A contribution to the herpetology of Arabia with a preliminary list of the reptiles and batrachians of Egypt. London: R. H. Porter, III+ 122 pp.
- Angel F & Lathe H. 1938. Reptiles et Amphibiens du Sahara et du Soudan. Bull. Com. Etud. hist. scient. Afr. occid. fr. 21: 345-384, 1 pl.
- Auliya M, Altherr S, Ariano-Sanchez D, Baard EH, Brown C, Brown RM, Cantu J-C, Gentile G, Gildenhuys P & Henningheim E. 2016. Trade in live reptiles, its impact on wild populations, and the role of the Europe-an market. Biol. Conserv., 204: 103–119.
- Bauer AM, De Boer JC & Taylor DJ. 2017. Atlas of the Reptiles of Libya. Proceedings of the California Academy of Sciences, 64(8): 155–318.
Bons J & Geniez P. 1996. Amphibiens et reptiles du Maroc (Sahara Occidental compris). Atlas Biogéographique. Asociacion Herpetologica Espanola, Barcelone. 319 pp. - Blanc CP & Shane MH. 1981. Proposition pour unk protection plus ample pour Ies reptiles et les amphibiens de Bou Hedma. Parks 1981, 6 (1): 15-18.
- Böhme W, Wilms T, Nickel H & Merz M. 2001.Bericht über einer herpetoogische Forschungsreise indie westliche Sahara und ihre Randgebiete. Zeitschrift Des Kölner Zoo, 44(3): 117-131.
- Boulenger GA. 1891. Catalogue of the reptiles and batrachians of Barbary (Morocco, Algeria, Tunisia), based chiefly upon the notes and collections made in 1880-1884 by M. Fernand Lataste. Trans. zool. Soc. Lond. 13: 93-164, pls 13-18.
- Carranza S, Arnold EN, Geniez P, Roca J, Mateo JA. 2008. Radiation, multiple dispersal and parallelism in the skinks, Chalcides and Sphenops (Squamata: Scincidae), with comments on Scincus and Scincopus and the age of the Sahara Desert. Molecular Phylogenetics and Evolution 46 (3): 1071-1094.
- Chenchouni H. 2012. Diversity assessment of vertebrate fauna in a wetland of hot hyperarid lands. АРИДНЫЕ ЭКОСИСТЕМЫ, том 18, № 4 (53), с. 73-85.
- Chirio L. 2009. Inventaire des reptiles de la région de la Réserve de Biosphère Transfrontalière du W (Niger/Bénin/Burkina Faso: Afrique de l’Ouest). Bulletin de la Société Herpétologique de France, 132: 13–41.
- Convention on International Trade in Endangered Species of Wild Fauna and Flora. 1973. Desarrollado mediante el Reglamento (CE) n.º 338/97 del Consejo, de 9 de diciembre de 1996, relativo a la protección de especies de la fauna y flora silvestres mediante el control de su comercio, y del Reglamento (CE) n.º 865/2006 de la Comisión, de 4 de mayo de 2006. Está basado en un sistema de permisos y certificados comerciales que pueden obtenerse si se cumple una serie de condiciones, y que deben ser presentados antes de que un envío de especímenes sea autorizado a entrar o salir de un país. establece un marco jurídico internacional para prevenir el comercio de especies en peligro de extinción y para regular eficazmente el comercio de otras especies de animales y plantas silvestres. Washington, 3 de marzo de 1973
- D’Cruze N, Assou D, Coulthard E, Norrey J, Megson D, Macdonald DW, Harrington LA, Ronfot D, Segniagbeto GH, Auliya M. 2020. Snake oil and pangolin scales: insights into wild animal use at “Marché des Fétiches” traditional medicine market, Togo. Nature Conservation, 39: 45–71.
- Dunger GT. 1973. The lizards and snakes of Nigeria. Part 7 – The skinks of Nigeria (continued and completed). Niger. Fld 38 (2): 54-80, 16 figs.
- Evans S. 2008. The skull of lizards and tuatara. In: Gaunt AS, Adler K, eds. The Skull of Lepidosauria. Ithaca: Society for the Study of Amphibians and Reptiles, 348.
- Faith DP & Walker PA. 2002.The role of trade-offs in biodiversity con-servation planning: linking local management, regional planning and global conservation efforts. Journal of Biosciences 27 (4): 393 – 4 07.
- Geniez P, Crochet P, Mateo-Miras J, Joger U, Pleguezuelos J, Slimani T & Baha El Din S. 2010. Scincopus fasciatus, Peters’ Banded Skink. The IUCN Red List of Threatened Species.
- Geniez P, Mateo JA, Geniez M & Pether J. 2004. The amphibians and reptiles of the Western Sahara (former Spanish Sahara) and adjacent regions. Edition Chimaira, Frankfurt, 228 pp.
- Gonçalves DV, Álvares F & Brito JC. 2013. Data on the distribution of herpetofauna of southern Niger with comments on Termit & Tin Toumma National Nature Reserve. Boletín de la Asociación Herpetológica Española, 24(1): 74.
- Griffith H, Ngo A & Murphy RW. 2000. A cladistic evaluation of the cosmopolitan genus Eumeces Wiegmann (Reptilia, Squamata, Scincidae). Russ. J. Herpetol. 7 (1): 1-16.
- Ineich I, Chirio L, Ascani M, Rabeil T & Newby J.2014 Herpetofauna of Termit Massif and neighbour áreas in Tenere Desert, southeastern Niger, West Africa. Herpetology Notes, volume 7: 375-390.
- Irrahim A & Ineich I. 2005. Additional records to the herpetofauna of Nalut Province, Libya. African Herp News, 38 (July 2005): 2-9.
- Kalboussi M. 2020. Scincopus fasciatus.(Banded Skink). Mating Behavior. Herpetological Review 51(3):603.
- Kalboussi M. 2021. Scincopus fasciatus, distribution and new records in Tunisia, Scientific Reports in Life Sciences 2(1), 52-57.
- Lanza B & Corsi M. 1981. Notes on Scincopus fasciatus (Peters) with a description of a new subspecies (Reptilia Scincidae). Monitore zoologico italiano, 14(3): 17–29
- Le Berre M. 1989. Faune du Sahara. Raymond Chabaud-Lechevalier, Paris.
- Ley 42/2007, de 13 de diciembre, del Patrimonio Natural y de la Biodiversidad. Boletín Oficial del Estado. España. 14 de diciembre de 2007.
- Martínez del Mármol G, Harris DJ, Geniez P, de Pous P & Salvi D. 2019. Amphibians and Reptiles of Morocco. Frankfurt, Germany, Edition Chimaira. 478 pp.
- Moorhouse TP, D’Cruze NC & Macdonald DW. 2021. Information About Zoonotic Disease Risks Reduces Desire to Own Exotic Pets Among Global Consumers. Front. Ecol. Evol. 9:609547.
- Nouira S, Blanc CP & Ktari MH. 1999. Biodiversité de l’herpétofaune tunisienne. III. Les Sincidae (Reptilia, Sauria). Bulletin de la Société les Sciences Naturelles de Tunisie, 27: 121–130.
- Papenfuss TJ. 1969. Preliminary analysis of the reptiles of arid central West Africa. Wasmann Journal of Biology, 27(3): 249–325.
- Perera A, Sampaio F, Costa S, Salvi D & Harris DJ. 2012. Genetic variability and relationships within the skinks Eumeces algeriensis and Eumeces schneideri using mitochondrial markers. African Journal of Herpetology 61 (1): 69-80.
- Pyron R, Burbrink F & Wiens J. 2013. A phylogeny and revised classification of Squamata, including 4161 species of lizards and snakes. BCM Evolutionary Biology, 13: 93.
- Rouagrachid M. 2012. Biodiversite de L’Hepetofaune Algerienne. Ministére de L’amenagement du territoire et de L’environnment.
- Sánchez Vialas A, Wong E, Lobón-Rovira J & García-Antón P. 2022 Scincopus fasciatus (Peter’s Banded Skink) reproductive biology. Herpetological Review 53(2):252-253.
- Schleich HH, Kästle W & Kabisch K. 1996. Amphibians and Reptiles of North Africa. Koeltz Sci. Books, Koenigstein. 630 pp.
- Sindaco R. 1995. Addition to the herpetofauna of Libya: Scincopus fasciatus fasciatus (Peters, 1864) (Reptilia: Scincidae). Bollettino del Museo Regionale di Scienze Naturali di Torino, 13(1): 117–122.
- Sow A, Gonçalves V, Sousa F, Martínez-Freiría F., Santarém F, Velo-Antón G, Dieng H, Campos J, Diagne S, Boratynski Z & Brito JC. 2017. Atlas of the distribution of amphibians and reptiles in the Diawling National Park, Mauritania. Basic and Applied Herpetology, 31: 101-116.
- Staudt K, Saxe F, Schmied H, Soeur R, Bohme W & Baumgartner W. 2012. Comparative investigations of the sandfish’s β-keratin (Reptilia: Scincidae: Scincus scincus). Part 1: Surface and molecular examinations. Journal of Biomimetics Biomaterials and Tissue Engineering 15:1-16.
- Toland E, Bando M, Hamer M, Cadenas V, Laidlaw R, Martínez-Silvestre A & van der Wielen P. 2020. Turning Negatives into Positives for Pet Trading and Keeping: A Review of Positive Lists. Animals, 10, 2371.
- Trape JF, Trape S & Chirio L. 2012. Lézards, crocodiles et tortues d’Afrique occidentale et du Sahara. IRD Orstom, 503 pp.
- Uetz P, Freed P & Hošek J. 2021. The reptile database. Available at http://www.reptile-database.org (accessed 20 May 2022).
- Velo-Anton G, Henrique M, Liz AV, Martínez-Freiría F, Pleguezuelos JM, Geniez P, Crochet P-A & Brito JC. 2022. DNA barcode reference library for the West Sahara-Sahel reptiles. nature.com/scientificdata/ 9:459. https://doi.org/10.1038/s41597-022-01582-1
- Vicent-Castelló P, Herrero-González D, Rodríguez-Lozano JJ, García-Antón P & Sánchez-Vialas A.2018. On the presence of Scincopus fasciatus (Squamata, Scincidae) in Mauritania. Boletín de la Asociación Herpetológica Española, 29(1): 56–58.
- Watanabe A, Fabre A, Felice R, Maisano J, Müller J, Herrel A & Goswami A. 2019. Ecomorphological diversification in squamates from conserved pattern of cranial integration. Proceedings of the National Academy of Sciences. 116. 201820967. 10.1073/pnas.1820967116.
- Werner F. 1919. Wissenschaftliche Ergebnisse der mit Untersrutzung der Kaiserlichen Akademie der Wissenschaften in Wien aus der Erbschaft Treitl von F. Werner unternommenen zoologischen expedition nach dem Anglo-Agyptischen Sudan (Kordofan) 1914. IV. Bearbeitung der Fische, Amphibien und Reptilien. Denkschr. Akad. Wiss., Wien (Math.-nat. Kl.) 96: 437-509, 8 figs, 2 pls, 1 map.
- Whiting AS, Bauer AM & Sites Jr JW. 2003. Phylogenetic relationships and limb loss in sub-Saharan African scincine lizards (Squamata: Scincidae). Molecular Phylogenetics and Evolution 582–598.
- Wickens. 1984. In: Cloudsley-Thompson J.L. (ed.), 1984. Sahara desert. Pergamon Press, Oxford, New York, etc.
- Wiens JJ, Brandley MC & Reeder TW. 2006. Why does a trait evolve multiple times within a clade? Repeated evolution of snakelike body form in squamate reptiles. Evolution 60:123–141.
- Yildirım E, Kumlutaş Y & Ilgaz Ç. 2015.A preliminary study of comparative osteology of the scincid lizard Eumesces schneideri (Daudin, 1802) (Squamata: Scincidae) subspecies in Anatolia. – Journal of Anatolian Natural Sciences, 6(1): 34– 43.
- Zheng Y & Wiens JJ. 2016. Combining phylogenomic and supermatrix approaches, and a time-calibrated phylogeny for squamate reptiles (lizards and snakes) based on 52 genes and 4162 species. Mol. Phylogen. Evol. 94, 537–547.
Para citar esta página: Pablo García Antón, Alberto Sánchez Vialas, Javier Lobón-Rovira, Fernando Iglesias &Teodoro Abbad (2023): Scincopus fasciatus (Peters, 1864). En: Martínez, G., León, R., Jiménez-Robles, O., González De la Vega, J. P., Gabari, V., Rebollo, B., Sánchez-Tójar, A., Fernández-Cardenete, J. R., Gállego, J. (Eds.). Moroccoherps. Anfibios y Reptiles de Marruecos. Disponible en www.moroccoherps.com/ficha/Scincopus_fasciatus/.
Para citar www.morocoherps.com en su conjunto: Martínez, G., León, R., Jiménez-Robles, O., González De la Vega, J.P., Gabari, V., Rebollo, B., Sánchez-Tójar, A., Fernández-Cardenete, J.R., Gállego, J. (Eds.). Moroccoherps. Amphibians and Reptiles of Morocco and Western Sahara. Available from www.moroccoherps.com

